Лабораторная работа

Комплексные соединения
1. Соединения с комплексным катионом
К растворам солей меди, никеля и цинка добавьте по каплям 10%‑ный раствор аммиака. Наблюдайте образование осадков. Полученные осадки растворите в избытке концентрированного раствора аммиака.
Составьте уравнения реакций, учитывая, что растворение осадков происходит за счет комплексообразования, при этом в образующихся комплексных катионах кч меди, никеля и цинка соответственно равны 6, 6 и 4. Назовите полученные комплексные соединения. Почему гидроксиды, содержащие комплексные ионы, являются сильными основаниями, а соответствующие им простые гидроксиды ‑ слабыми?
Опишите строение полученных аммиачных комплексов рамках ТКП: 1) рассчитайте ЭСКП, сравните радиусы катионов Cu2+, Ni2+, Zn2+ и длины связей в полученных комплексах; 2) объясните наличие или отсутствие окраски; 3) различаются ли магнитные свойства полученных комплексов?
Раствор с аммиачным комплексом меди сохраните для опыта 3.
2. Соединения с комплексным катионом
К 1 мл раствора нитрата ртути (II) добавьте сначала по каплям, а затем избыток концентрированного раствора иодида калия. Наблюдайте растворение выпадающего в первый момент осадка.
Составьте уравнения реакций, учитывая, что растворение осадка происходит за счет образования тетраэдрического комплекса ртути. Опишите строение полученного комплексного иона в рамках МВС и ТКП и дайте название.
Такой же опыт можно провести, заменив раствор соли ртути раствором соли висмута.
Раствор сохраните для опыта 3.
3. Поведение комплексных ионов в растворе
а) Разрушение внутренней сферы комплексов за счет образования осадков
Растворы, полученные в результате опытов 1 и 2, разделите на две части и добавьте к ним растворы NaOH и Na2S. Выпадают ли осадки?
Напишите уравнения реакций в молекулярной и ионной форме и докажите наличие или отсутствие осадков расчетом Кравн. проведенных реакций.
б) Разрушение внутренней сферы комплексов за счет образования более устойчивых комплексных ионов
К раствору нитрата серебра добавьте избыток концентрированного раствора хлорида натрия. Полученный осадок разделите на три части и подействуйте на них концентрированными растворами аммиака, тиосульфата натрия и нитрита натрия. Разрушается ли полученный комплексный ион?
Составьте уравнения реакций в молекулярной и ионной форме (кч(Ag)=2) и подтвердите результаты опыта расчетом Кравн. проведенных реакций.
4. Окраска комплексов
а) Сравнение окраски безводных солей и кристаллогидратов
В отдельных тиглях нагрейте кристаллические вещества CoCl2*6H2O, CuSO4*5H2O, NiSO4*7H2O, наблюдайте изменение окраски за счет образования безводных солей. После охлаждения тиглей добавьте по каплям воду; как при этом изменилась окраска?
Составьте уравнения реакций и объясните изменение окраски за счет изменения природы лигандов, окружающих данный комплексообразователь.
б) Сравнение окраски комплексов кобальта (+2)
К водному раствору соли кобальта, содержащему аквакомплексы [Co(H2O)6]2+, в отдельных пробирках добавьте концентрированную соляную кислоту и кристаллический роданид аммония. Наблюдайте изменение окраски за счет комплексообразования.
Составьте уравнения реакций с учетом того, что в полученных комплексных соединениях кч(Со) = 4. Объясните изменение окраски за счет изменения природы и симметрии поля лигандов, окружающих данный комплексообразователь. Почему окраска изменилась с розовой на синюю (а, например, не наоборот)?
5. Комплексы с полидентатными лигандами
В пробирке по обменной реакции получите гидроксид железа (III) и добавьте к осадку концентрированный раствор щавелевой (НООС‑СООН) кислоты. Составьте уравнение реакции, изобразите структурную формулу полученного комплексного соединения, учитывая, что гидрооксалат‑ион является бидентатным лигандом, дайте название комплексному соединению.
Полученный раствор разделите на две части и подействуйте на него растворами роданида аммония и гексацианоферрата (II) калия. Обнаруживается ли в растворе присутствие несвязанных ионов Fe+3 (приведите количественные доказательства)? Составьте уравнения.
6. Влияние комплексообразования на окислительно‑восстановительные свойства веществ
Стандартный red‑ox‑потенциал для аквокомплексов железа существенно отличается от этой величины для цианидных комплексов:
φ0 ([Fe(H2O)6]3+/[Fe(H2O)6]2+) = 0,77 B
φ0 ([Fe(CN)6]3‑/[Fe(CN)6]4‑) = 0,36 B
По значениям φ0 определите, какие ионы ‑ [Fe(H2O)6]2+ или [Fe(CN)6]4‑ ‑ могут быть окислены йодной водой в стандартных условиях (φ0 (I2/2I‑) = 0,54 B); ответ подтвердите экспериментально. Составьте уравнение реакции.
| Kнест. | |
| [Ag(NH3)2]+ | 5,8*10‑8 |
| [Ag(S2O3)2]3‑ | 1*10‑13 |
| [HgI4]2‑ | 1*10‑30 |
| [BiI4]‑ | 1,1*10‑15 |
| [Cu(NH3)4(H2O)2]2+ | 2*10‑13 |
| [Ni(NH3)6]2+ | 2*10‑9 |
| [Zn(NH3)4]2+ | 4*10‑10 |
| [Fe(CN)6]3‑ | 1*10‑31 |
| [Fe(CN)6]4‑ | 1*10‑24 |
| [Fe(SCN)6]3‑ | 5,9*10‑4 |
| [Fe(HC2O4)3] | 6,3*10‑21 |
| ПР | |
| AgCl | 1,8*10‑10 |
| Ag2O | 1,95*10‑8 |
| Ag2S | 6*10‑50 |
| HgO | 3*10‑26 |
| HgS | 3*10‑53 |
| CuS | 6*10‑36 |
| Cu(OH)2 | 8,3*10‑20 |
| Ni(OH)2 | 2*10‑15 |
| Zn(OH)2 | 1,4*10‑17 |
| BiI3 | 8,1*10‑19 |
| Bi2S3 | 1,6*10‑72 |
| Bi(OH)3 | 4,3*10‑31 |
7. Гидратная изомерия комплексных соединений
Несколько фиолетовых кристаллов CrCl3*6H2O растворите в воде и нагрейте полученный фиолетовый раствор. Почему окраска раствора изменяется на зеленую? Составьте схему перехода и назовите все комплексные соединения.
Таблица растворимости веществ в воде при комнатной температуре
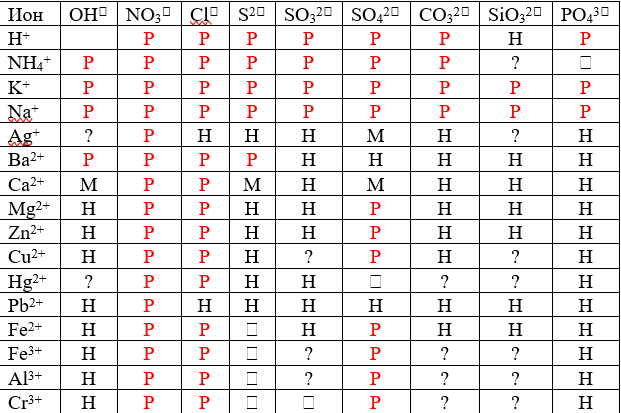
Вещество:
“Р” растворимо,
“Н” нерастворимо,
“М” малорастворимо,
“ “ в водной среде разлагается,
“?” – нет данных о существовании соединения.
Электрохимический ряд активности металлов
| ‑3,08 | ‑3,02 | ‑2,99 | ‑2,92 | ‑2,90 | ‑2,89 | ‑2,87 | ‑2,71 | ‑2,37 | ‑2,34 | ‑1,7 | ‑1,67 | ‑1,05 | ‑0,76 | ‑0,71 | ‑0,44 | ‑0,40 | ‑0,28 | ‑0,25 | ‑0,14 | ‑0,13 | 0 | +0,34 | +0,8 | +0,83 | +0,85 | +1,2 | +1,7
|
| Cs | Li | Rb | K | Ba | Sr | Ca | Na | La | Mg | Be | Al | Mn | Zn | Cr | Fe | Cd | Co | Ni | Sn | Pb | H | Cu | Ag | Pd | Hg | Pt | Au |
или напишите нам прямо сейчас:

Здравствуйте. Скажите пожалуйста, планирую поступать в магистратуру на факультет Психологии « Психология личности»в РГГУ скажите пожалуйста, есть ли у вас, ответы на вступительные экзамены? так как, планирую, сделать акцент на бюджет. Спасибо.
Арсений, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Дистанционная помощь в защите ВКР
Анастасия, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Здравствуйте. Нужна срочно практическая часть вкр, третья глава. Скину похожие работы, на которые можно ориентироваться
Александр, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
вкр по теме: экологический туризм России : анализ состояния, проблемы и перспективы
Людмила, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Здравствуйте вы защищаете ВКР?
Ольга, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Написать магистерскую ВКР на тему «Совершенствование логистических бизнес-процессов на примере торговой компании». Не менее 100 страниц.
Миша, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Здравствуйте нужна работа Вкр
Лена, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Написать ВКР 3 раздела Тема строительство строительство жилого дома с применением каркасно-монолитных технологий Антиплагиат от 75% ПЗ и чертежи
Владимир, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.