Лабораторная работа

Гальванический элемент. Направление протекания окислительно-восстановительных реакций. Электрохимическая коррозия. Электролиз
1. Гальванический элемент
Из указанных преподавателем металлов и их растворов соберите гальванический элемент (рис.5).
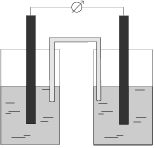 Рис.5. Схема гальванического элемента
Рис.5. Схема гальванического элемента
Для этого два небольших стаканчика на 3/4 наполните 1М растворами указанных солей и опустите в них пластины соответствующих металлов, соединенные металлическим проводником. Стаканы с растворами соедините солевым мостиком ‑ стеклянной трубкой, заполненной раствором хлорида калия. Отметьте по вольтметру напряжение.
Рассчитайте ожидаемое значение ЭДС для каждого гальванического элемента, использованного в опыте. Составьте схемы гальванических элементов, указав катод и анод и направление движения тока в цепи.
Как изменится ЭДС гальванического элемента, если один из растворов солей разбавить в 10 раз? Рассчитайте ЭДС для данного случая и измерьте, разбавив соответствующий раствор в 10 раз. Вновь сравните расчетное и экспериментальное значения. Как следует изменять концентрацию раствора в прикатодном пространстве (в прианодном пространстве), чтобы повысить ЭДС гальванического элемента?
2. Направление протекания окислительно‑восстановительных реакций
Пользуясь таблицами стандартных электродных потенциалов, рассчитайте ЭДС окислительно‑восстановительной реакции между ионами Fe3+ и Г‑ (где Г = Cl, Br, I) и сделайте вывод о возможности восстановления ионов Fe3+ каждым из галогенид‑ионов.
Расчеты проверьте на опыте. В три пробирки налейте по 2 мл 2М растворов хлорида, бромида и иодида калия, затем в каждую из них добавьте равные объемы 2М раствора хлорида железа (III). Что наблюдается? Согласуются ли данные опыта с расчетом? Если нет, то почему? Что нужно изменить в условиях проведения опыта, чтобы расчетные и экспериментальные данные совпали?
Сделайте следующий расчет, имеющий отношение к проведенному опыту, и его результат используйте для комментария вашего эксперимента: начиная с какой концентрации бромид‑ионов восстановление ионов Fe3+ термодинамически возможно, если [Fe3+] = 1 моль/л и [Fe2+] = 10‑6 моль/л.
| Полуреакция | φ0, B |
| Na+ + e → Na0 | ‑2,713 |
| K+ + e → K0 | ‑2,923 |
| Al3+ + 3e →Al0 | ‑1,66 |
| Cu2+ + 2e → Cu0 | 0,345 |
| Fe2+ + 2e → Fe0 | ‑0,44 |
| Ni2+ + 2e → Ni0 | ‑0,228 |
| Sn2+ + 2e → Sn0 | ‑0,136 |
| Zn2+ + 2e → Zn0 | ‑0,764 |
| Fe3+ + e → Fe2+ | 0,77 |
| Cl2 + 2e → 2Cl‑ | 1,359 |
| Br2 + 2e → 2Br‑ | 1,087 |
| I2 + 2e → 2I‑ | 0,536 |
| 2H+ + 2e → H2 | 0 |
| 2H2O + 2e → H2 + 2OH‑ | ‑0,828 |
| O2 + 2H2O + 4e → 4OH‑ | 0,401 |
| O2 + 4H+ + 4e → 2H2O | 1,229 |
| S2O82‑ + 2e → 2SO42‑ | 2,01 |
3. Коррозия
1) Влияние гальванопар на скорость коррозии металлов
а) В стеклянную V‑образно изогнутую трубку налейте 0,1 М раствор серной кислоты. Поместите в одно колено трубки полоску меди, в другую ‑ полоску цинка, пока не приводя их в соприкосновение. На какой из пластинок наблюдается выделение пузырьков газа и почему? Теперь приведите пластинки в контакт. Как изменилась скорость выделения газа и с какой пластинки он выделяется теперь? Как и почему отражается контакт двух металлов на скорости их коррозии? Составьте уравнения катодного и анодного процессов.
б) В пробирку налейте 1‑2 мл 0,1 М раствора серной кислоты и поместите туда кусочек цинка. Наблюдайте выделение водорода, обратите внимание на интенсивность этого процесса. Теперь добавьте в пробирку 2‑3 капли раствора сульфата меди. Как изменилась скорость выделения водорода? Объясните наблюдаемое образованием микрогальванопар, составьте уравнения катодного и анодного процессов.
2) Протекторная защита
В одной пробирке смешайте 5‑6 мл 1 М раствора уксусной кислоты и 0,5 мл раствора иодида калия. Содержимое пробирки разлейте на две части, затем одновременно в одну из них поместите кусочек свинца, в другую ‑ свинец в контакте с цинком. В какой пробирке раствор приобретает более интенсивную желтую окраску и почему? Объясните результаты опыта, составьте уравнения катодного и анодного процессов. Какой способ защиты от коррозии моделирует данный опыт?
3) Коррозия оцинкованного и луженого железа
В две пробирки налейте 3‑4 мл 0,1 М раствора серной кислоты, добавьте в каждую из них 2‑3 капли раствора гексацианоферрата(III) калия и опустите полоски оцинкованного и луженого железа, сделав предварительно на них глубокие царапины. В какой пробирке и почему появляется интенсивно‑синее окрашивание? Составьте уравнения катодного и анодного процессов для каждого случая. Какое покрытие является катодным? анодным? Сравните эффективность катодного и анодного покрытий.
4) Пассивирование стали
Зачистите наждаком два гвоздя. Один гвоздь пассивируйте, опустив его в пробирку с концентрированным раствором азотной кислоты. Ополосните гвоздь водой и вновь опустите в тот же раствор, после чего гвоздь достаньте и сполосните водой.
Обработанный и необработанный концентрированной кислотой гвоздь поместите в две пробирки с разбавленным раствором серной кислоты. В каком случае скорость выделения газа (какого?) больше?
5) Термическое оксидирование (воронение) стали
Очистите наждаком две стальные пластинки. Проведите оксидирование одной из них, для чего нагрейте пластинку в пламени горелки до появления цветов побежалости, т.е. до появления оксидных пленок, которые ввиду своей различной толщины вызывают интерференцию света и потому окрашиваются в разные цвета. Нанесите по капле раствора сульфата меди на оксидированный и неоксидированный образцы и по скорости появления пятна меди оцените защитные свойства образовавшейся пленки.
4. Электролиз растворов
а) Электролиз водных растворов иодида калия и сульфата натрия
Пользуясь величинами стандартных электродных потенциалов, предскажите состав продуктов электролиза водных растворов иодида калия и сульфата натрия. Составьте уравнения катодных и анодных процессов, суммарные уравнения с разделенными катодным и анодным пространствами и при перемешивании растворов. Предложите способы обнаружения продуктов электролиза.
В U‑образную трубку (рис.6) налейте раствор одной из солей, опустите в оба колена графитовые электроды, подсоединенные к внешнему источнику постоянного электрического тока. Включите прибор и подайте напряжение на электроды. Что наблюдается? Обнаружьте продукты электролиза предложенными способами.
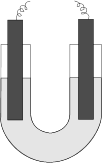 Рис.6. Схема электролизера с графитовыми электродами
Рис.6. Схема электролизера с графитовыми электродами
б) Влияние перенапряжения на состав продуктов электролиза
Используя данные по стандартным электродным потенциалам и учитывая перенапряжение по водороду и кислороду, обоснуйте состав продуктов электролиза водного раствора хлорида цинка. Как обнаружить ожидаемые продукты? Составьте уравнения катодных и анодных процессов, суммарные уравнения с разделенными катодным и анодным пространствами и при перемешивании раствора.
Проведите электролиз раствора хлорида цинка на графитовых электродах так же, как в предыдущем опыте, обнаружьте продукты электролиза.
в) Влияние материала анода на состав продуктов электролиза
Обоснуйте состав продуктов при электролизе раствора серной кислоты на медном аноде. Составьте уравнения катодных и анодных процессов, суммарное уравнение. Какое практическое значение может иметь электролиз, идущий по такой схеме?В большой стакан (рис.7) налейте 1М раствор серной кислоты и закройте его крышкой с закрепленными в ней графитовым и медным электродами.
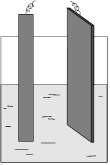 Рис.7. Схема электролизера с медным анодом
Рис.7. Схема электролизера с медным анодом
Подсоедините электроды к внешнему источнику постоянного тока так, чтобы медный электрод поляризовался анодно. Включите питание, подайте напряжение на электроды. Что наблюдается? Почему на графитовом электроде водород и медь выделяются одновременно?
После окончания опыта графитовый электрод погрузите в 10%‑ный раствор азотной кислоты (зачем?), после чего промойте водой.
или напишите нам прямо сейчас:

Здравствуйте. Скажите пожалуйста, планирую поступать в магистратуру на факультет Психологии « Психология личности»в РГГУ скажите пожалуйста, есть ли у вас, ответы на вступительные экзамены? так как, планирую, сделать акцент на бюджет. Спасибо.
Арсений, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Дистанционная помощь в защите ВКР
Анастасия, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Здравствуйте. Нужна срочно практическая часть вкр, третья глава. Скину похожие работы, на которые можно ориентироваться
Александр, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
вкр по теме: экологический туризм России : анализ состояния, проблемы и перспективы
Людмила, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Здравствуйте вы защищаете ВКР?
Ольга, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Написать магистерскую ВКР на тему «Совершенствование логистических бизнес-процессов на примере торговой компании». Не менее 100 страниц.
Миша, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Здравствуйте нужна работа Вкр
Лена, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Написать ВКР 3 раздела Тема строительство строительство жилого дома с применением каркасно-монолитных технологий Антиплагиат от 75% ПЗ и чертежи
Владимир, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.