Лабораторная работа

Химическая кинетика. Химическое равновесие
1. Зависимость скорости реакции от концентрации реагирующих веществ
Зависимость скорости реакции от концентрации можно исследовать на примере реакции тиосульфата натрия с серной кислотой:
Na2S2O3 + H2SO4 = Na2SO4 + H2O + SO2 + S↓
Появление мелкокристаллической серы вызывает опалесценцию (помутнение) раствора. По этому признаку можно косвенно судить о скорости протекающей реакции. В три большие пробирки (или стаканы объемом 50 мл) налейте по 5 мл 0,25 М раствора H2SO4, а в три другие нумерованные пробирки налейте 0,5 М раствор Na2S2O3: в первую ‑ 5 мл, во вторую ‑ 10 мл, в третью ‑ 15 мл. При этом необходимо воспользоваться разными цилиндрами, маркированными соответственно буквами «К» и «Т». Затем к содержимому первой пробирки добавьте 10 мл воды, а второй ‑ 5 мл воды
.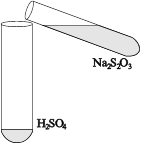 Рис.2. Порядок сливания реагентов (для быстрого и лучшего перемешивания
Рис.2. Порядок сливания реагентов (для быстрого и лучшего перемешивания
Быстро прилейте к кислоте подготовленные растворы и энергично перемешайте. По секундомеру определите время (τ, сек) с момента добавления кислоты до начала появления слабой опалесценции.
Рассчитайте концентрации растворов тиосульфата натрия, использованных в опыте, и условную скорость реакции как v=1/τ.
Данные опыта и результаты расчетов внесите в таблицу:
| № опыта |
объем растворов, мл |
концентрация раствора Na2S2O3, моль/л | время до начала помутнения раствора τ, сек | скорость реакции
v=1/τ, сек‑1 |
||
| Na2S2O3 | H2SO4 | H2O | ||||
| 1. | ||||||
| 2. | ||||||
| 3. | ||||||
Постройте график зависимости скорости реакции от концентрации тиосульфата натрия. При построении графика следует использовать четыре точки. (Четвертая точка должна соответствовать нулевой концентрации этого вещества).
Как с точки зрения закона действия масс должен выглядеть данный график (кривая, прямая, ломаная линия или др.)? График по своим экспериментальным точкам постройте с учетом этих теоретических представлений.
Сделайте вывод о влиянии концентрации реагирующих веществ на скорость химической реакции.
2. Зависимость скорости реакции от температуры
Для опыта возьмите растворы тиосульфата натрия и серной кислоты тех же концентраций, что и в опыте 1. Налейте в три нумерованные пробирки по 5 мл раствора Na2S2O3, а в другие три ‑ по 5 мл раствора H2SO4. Сгруппируйте пробирки в три пары (кислота ‑ тиосульфат). Первую пару поместите в стакан с водой, имеющей комнатную температуру, и выдержите минуты 3‑5 для выравнивания температуры (температуру контролировать термометром, погруженным в стакан с раствором кислоты). После этого растворы слейте и зафиксируйте время (τ, сек) до появления опалесценции. Вторую пару пробирок прогрейте в стакане с теплой водой до температуры, примерно на 10°С превышающей комнатную, и повторите опыт. Последнюю пару пробирок поместите в стакан со льдом и охладите до температуры примерно на 10°С ниже комнатной и вновь измерьте скорость реакции.
Данные опыта внесите в таблицу:
| № опыта |
объем растворов, мл |
температура t, °С |
время до начала помутнения раствора τ, сек | скорость реакции
v=1/τ, сек‑1 |
|
| Na2S2O3 | H2SO4 | ||||
| 1. | |||||
| 2. | |||||
| 3. | |||||
Выполните необходимые расчеты и постройте график в координатах «v=1/τ» от «t»(°C). Можно ли что‑то определенное сказать относительно скорости данной реакции при 0°C, можно ли и эту точку использовать для построения графика?
Рассчитайте температурный коэффициент скорости реакции. Сделайте вывод о зависимости скорости реакции от температуры, о количественном соответствии этой зависимости правилу Вант‑Гоффа. Объясните полученный результат.
Используя правило Вант‑Гоффа и уравнение Аррениуса, установите взаимосвязь между энергией активации и температурным коэффициентом скорости реакции. Рассчитайте Eакт. и прокомментируйте полученный результат.
3. Катализ
1. Каталитическое разложение пероксида водорода
Проследите влияние различных катализаторов на скорость реакции разложения пероксида водорода
2H2O2 → 2H2O + O2↑
а) Гетерогенный катализ. Налейте в две пробирки по 1 мл раствора индиго. В первую добавьте немного оксида марганца (IV) MnO2, во вторую ‑ столько же оксида свинца (IV) РbО2. В обе пробирки прилейте по 3 мл 3‑5%‑ного раствора перекиси водорода. В обеих пробирках происходит разложение перекиси водорода, при этом кислород, являющийся в момент выделения атомарным, обесцвечивает индиго. В какой из пробирок обесцвечивание проходит быстрее? Какой из катализаторов эффективнее влияет на скорость разложения пероксида водорода?
б) Гомогенный катализ. К 1‑2 мл раствора бихромата калия добавьте 1‑2 мл раствора пероксида водорода. Наблюдайте изменение окраски за счет образования неустойчивого пероксосоединения хрома CrO(O2)2. Составьте уравнение первой стадии реакции.
Теперь пробирку с раствором поместите в стакан с горячей водой. Как при этом изменяется окраска раствора? Какой газ выделяется? Напишите уравнение второй стадии.
Сделайте вывод о роли К2Cr2O7 в данной реакции. Какая из стадий этого процесса является лимитирующей? С учетом этого изобразите энергетическую диаграмму данной каталитической реакции.
В чем сущность влияния катализаторов на скорость химических реакций?
2. Автокатализ
В две пробирки налейте по 2 мл насыщенного раствора щавелевой кислоты, добавьте по нескольку капель разбавленной серной кислоты и раствора перманганата калия, а затем в одну из пробирок внесите несколько капель раствора сульфата марганца (II). В какой из пробирок обесцвечивание перманганата идет быстрее? Составьте уравнение. В чем роль сульфата марганца (II)? Какие реакции называются автокаталитическими?
4. Зависимость скорости реакции от природы реагирующих веществ
Вам предлагаются литий и калий (в склянках под слоем керосина), кристаллизатор с водой, пинцет, скальпель, фильтровальная бумага. Предложите схему эксперимента, в котором проявилась бы зависимость скорости химической реакции от природы реагирующих веществ. Как на предварительных этапах опыта получить информацию о разной химической активности металлов и, соответственно, предположить и обосновать различие в скоростях реакций?
5. Влияние площади соприкосновения реагирующих веществ на скорость гетерогенной химической реакции
Уравновесьте на технохимических весах кусочек мрамора массой примерно 0,5 г порошком мрамора. В две пробирки налейте по 3‑5 мл раствора разбавленной соляной кислоты и внесите в них одновременно навески мрамора. Отметьте время, которое требуется для полного растворения мрамора в каждом случае. Сделайте вывод о влиянии площади поверхности контакта реагирующих веществ на скорость химической реакции.
6. Способы смещения химического равновесия
а) Влияние концентрации реагирующих веществ на химическое равновесие
Для этого опыта удобно использовать следующую обратимую реакцию
FeCl3 + 3 KCNS ⇔ Fe(CNS)3 + 3KCl
(или, более точно:
[Fe(H2O)6]+3 + xSCN‑ + yCl‑ ⇔[Fe(H2O)6‑x‑y(SCN)xCly ]+(3‑x‑y) + (x+y)H2O)
В этой системе только роданид железа Fe(CNS)3 (точнее, [Fe(H2O)6‑x‑y(SCN)xCly ]+(3‑x‑y)) имеет интенсивную красную окраску, в то время как роданид калия и хлорид калия бесцветны, а хлорид железа (III) в разбавленном растворе имеет слабо желтую окраску. Поэтому по интенсивности красного окрашивания раствора можно делать вывод о концентрации роданида железа и, следовательно, о положении равновесия в данной системе.
В пробирку с 2‑3 мл разбавленного раствора хлорида железа (III) прилейте немного раствора роданида аммония до приобретения раствором слабо красного окрашивания. Полученный раствор разделите на четыре части. Одну оставьте для сравнения, во вторую долейте равный объем раствора хлорида железа, в третью ‑ равный объем раствора роданида калия, в четвертую добавьте 1‑2 стеклянные ложечки кристаллического хлорида калия.
На основании принципа Ле Шателье объясните наблюдаемые явления. Как оказанные воздействия влияют на скорость прямой и обратной реакций?
Составьте выражение для константы равновесия данной реакции и с помощью его обоснуйте смещение равновесия.
В каком из первых двух случаев сильнее меняется интенсивность окраски раствора и почему? Нарушится ли равновесие в системе (почему, как?) при разбавлении раствора (скажем, вдвое).
б) Влияние температуры на химическое равновесие
Вам предлагается закрытая (или изолированная?) система, содержащая газовую смесь оксида азота (IV) NO2 и его димера ‑ N2O4 (рис.3). В системе имеет место химическое равновесие: NO2 ⇔ N2O4, τН = ‑54 кДж
О соотношении концентраций газов, а следовательно о положении равновесия реакции, можно судить по окраске: NO2 имеет темно‑бурый цвет, а N2O4 практически бесцветен.
На основании анализа уравнения реакции сделайте вывод о том, в какую сторону сместится химическое равновесие при нагревании (охлаждении) системы. Как это отразится на окраске газовой смеси
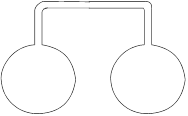 Рис.3. Сосуд с газовой смесью оксида азота (IV) и его димера
Рис.3. Сосуд с газовой смесью оксида азота (IV) и его димера
Одну из колб прибора опустите в стакан с горячей водой, а вторую ‑ в стакан с охлажденной. Объясните наблюдаемые явления. Выньте сосуды из стаканов. Что происходит? Как изменяются скорости обеих реакций при нагревании? Какая из них имеет больший температурный коэффициент скорости? Ответ обоснуйте.
или напишите нам прямо сейчас:

Здравствуйте. Скажите пожалуйста, планирую поступать в магистратуру на факультет Психологии « Психология личности»в РГГУ скажите пожалуйста, есть ли у вас, ответы на вступительные экзамены? так как, планирую, сделать акцент на бюджет. Спасибо.
Арсений, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Дистанционная помощь в защите ВКР
Анастасия, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Здравствуйте. Нужна срочно практическая часть вкр, третья глава. Скину похожие работы, на которые можно ориентироваться
Александр, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
вкр по теме: экологический туризм России : анализ состояния, проблемы и перспективы
Людмила, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Здравствуйте вы защищаете ВКР?
Ольга, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Написать магистерскую ВКР на тему «Совершенствование логистических бизнес-процессов на примере торговой компании». Не менее 100 страниц.
Миша, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Здравствуйте нужна работа Вкр
Лена, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Написать ВКР 3 раздела Тема строительство строительство жилого дома с применением каркасно-монолитных технологий Антиплагиат от 75% ПЗ и чертежи
Владимир, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.