Лабораторная работа

Химическая термодинамика
1. Определение изменения энтальпии реакции нейтрализации
Для проведения эксперимента необходимо взять (по указанию преподавателя) один из растворов сильной кислоты (HCl, H2SO4, HNO3) и один из растворов щелочи (NaOH, KOH) заданных концентраций. Составьте уравнение реакции между указанными кислотой и щелочью в молекулярном и ионном виде.
Опыт проводят в калориметрической установке, упрощенная схема которой показана на рисунке 1. Установка состоит из двух алюминиевых стаканов, вставленных один в другой и изолированных друг от друга корковыми или резиновыми прокладками в целях уменьшения потерь тепла. Во внутренний стакан калориметра помещается стеклянный химический стакан, в котором и проводится опыт.
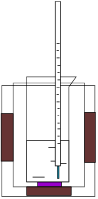
Рис.1. Схема калориметрической установки
Взвесьте калориметрический стеклянный стакан. Измерьте его диаметр и высоту с точностью до 1 мм. При помощи мерных цилиндров точно отмерьте равные объемы (20‑25 мл, объем указывает преподаватель) растворов кислоты и щелочи равных концентраций; при этом необходимо воспользоваться разными цилиндрами, маркированными соответственно буквами «К» и «Щ». В стеклянный стакан калориметра, предварительно вытащив его из калориметрической установки, аккуратно, без потерь, внесите отмеренный объем раствора щелочи. Стакан с раствором щелочи вновь поместите в калориметрическую установку. Измерьте температуру раствора кислоты при помощи ртутного термометра с точностью до 0,10С. Ополоснув термометр дистиллированной водой, c той же точностью измерьте температуру раствора щелочи, находящегося в стеклянном стакане калориметра. Не вынимая термометра из раствора щелочи, быстро и без потерь прилейте к нему весь раствор кислоты. При помощи термометра аккуратно перемешайте полученный раствор и отметьте максимальную температуру, которую покажет термометр. После этого вытащите стеклянный стакан из калориметрической установки и измерьте высоту столба жидкости в нем. С помощью ареометра измерьте плотность полученного раствора.
Результаты опыта внесите в таблицу.
На основании полученных данных рассчитайте изменение энтальпии реакции нейтрализации.
| Кислота | Щелочь | tнач.,°С растворов кислоты и щелочи до начала опыта
(tК + tЩ)/2 |
tкон..,°С
раствора после проведения реакции нейтрализации |
r, г/см3
раствора после проведения реакции нейтрализации |
Стакан | |||||||
| СМ, моль/л | V, мл | tК,°С до начала опыта | СМ, моль/л | V, мл | tЩ,°С до начала опыта | масса, г | диаметр, см | высота, см | высота столба жидкости после опыта, см | |||
Пояснение к расчетам:
Вычисление теплоты, выделившейся в ходе опыта, проводится по формуле:
Q = (mр‑раСр‑ра + mстеклаСстекла)Δt (Дж),
где Δt = tкон. – tнач; Ср‑ра и Сстекла – удельные теплоемкости раствора (Ср‑ра примем равной теплоемкости воды, Своды = 4,184 Дж/г К) и стекла (Сстекла = 0,753 Дж/г К); mр‑ра и mстекла – массы раствора после проведения реакции и стакана, занятого раствором. Массу раствора можно определить, зная его плотность и объем (определяем как сумму объемов исходных растворов кислоты и щелочи, при этом, правда, пренебрегаем контракцией). Массу стакана, занятого раствором, можно оценить по пропорции, предварительно вычислив его общую площадь и площадь, занятую раствором.
2. Зная концентрации и объемы исходных растворов, вычислить количества n кислоты и щелочи, взятые для проведения реакции. По найденной величине сделать пересчет выделившегося количества тепла на 1 моль Н+ (ОН‑).
3. Рассчитать значение изменения энтальпии реакции нейтрализации по табличным данным (ΔНобр.0(Н+) = 0, ΔНобр.0(ОН‑) =‑230,19, ΔНобр.0(Н2О(ж)) = ‑285,83 кДж/моль). Определить (в %) относительную ошибку опыта.
Почему реакция нейтрализации сопровождается выделением тепла? Почему тепловой эффект реакции нейтрализации сильного основания сильной кислотой не зависит от природы кислоты и основания? относится ли то же самое к слабым кислотам и основаниям и почему?
2. Определение вероятности протекания реакции
Составьте молекулярные и ионные уравнения реакций растворения сульфидов марганца, железа, меди и цинка в разбавленной серной кислоте и, выполнив по данным таблицы необходимые расчеты, определите, растворение каких сульфидов термодинамически вероятно, а каких – нет.
Пользуясь растворами солей марганца, железа, меди и цинка и раствором сульфида натрия, осадите в четырех пробирках указанные сульфиды, осадки промойте дистиллированной водой методом декантации, а затем добавьте к каждому из них 2‑3 мл разбавленного раствора серной кислоты. Что происходит? Сравните данные опыта с результатами расчета.
| ΔG0f, кДж/моль | |
| Mn2+ | ‑227,1 |
| Fe2+ | ‑78,96 |
| Cu2+ | 65,61 |
| Zn2+ | ‑147,26 |
| MnS | ‑219,36 |
| FeS | ‑100,8 |
| CuS | ‑53,6 |
| ZnS | ‑200,7 |
| H2S | ‑27,9 |
| H2O | ‑237,24 |
3. Выбор направления протекания реакции
Между ионами Э3+ и S2‑ в водном растворе возможно либо обменное взаимодействие, либо взаимно усиливающийся гидролиз, либо окислительно‑восстановительная реакция, если степень окисления +3 у элемента не слишком устойчива и может понижаться до +2:
2Э3+ + 3S2‑ → Э2S3
2Э3+ + 3S2‑ + 6Н2О →2Э(ОН)3 + 3Н2S
2Э3+ + 3S2‑ → 2ЭS + S
Пользуясь данными таблицы, выполните необходимые расчеты и выясните, какой из этих вариантов реакций наиболее термодинамически вероятен при взаимодействии сульфида натрия с солями трехзарядных катионов железа, алюминия, хрома и висмута. По каким внешним признакам в каждом конкретном случае можно определить, по какому пути пошла реакция?
В три пробирки налейте по 1‑2 мл растворов указанных солей и добавьте по 1 мл раствора сульфида натрия. Что наблюдается в каждом случае? Совпадает ли прогноз с результатами опыта?
| ΔG0f, кДж/моль | |
| Fe3+ | ‑18 |
| Al3+ | ‑490,5 |
| Cr3+ | ‑223,2 |
| Bi3+ | 91,9 |
| S2‑ | 92,47 |
| FeS | ‑100,8 |
| CrS | ‑ |
| Fe2S3 | ‑ |
| Cr2S3 | ‑ |
| Bi2S3 | ‑152,9 |
| Al2S3 | ‑492,5 |
| Fe(OH)3 | ‑699,6 |
| Cr(OH)3 | ‑849,02 |
| Bi(OH)3 | ‑580,3 |
| Al(OH)3 | ‑1157 |
| H2S | ‑27,9 |
| H2O | ‑237,24 |
или напишите нам прямо сейчас:

Здравствуйте. Скажите пожалуйста, планирую поступать в магистратуру на факультет Психологии « Психология личности»в РГГУ скажите пожалуйста, есть ли у вас, ответы на вступительные экзамены? так как, планирую, сделать акцент на бюджет. Спасибо.
Арсений, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Дистанционная помощь в защите ВКР
Анастасия, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Здравствуйте. Нужна срочно практическая часть вкр, третья глава. Скину похожие работы, на которые можно ориентироваться
Александр, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
вкр по теме: экологический туризм России : анализ состояния, проблемы и перспективы
Людмила, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Здравствуйте вы защищаете ВКР?
Ольга, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Написать магистерскую ВКР на тему «Совершенствование логистических бизнес-процессов на примере торговой компании». Не менее 100 страниц.
Миша, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Здравствуйте нужна работа Вкр
Лена, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.
Написать ВКР 3 раздела Тема строительство строительство жилого дома с применением каркасно-монолитных технологий Антиплагиат от 75% ПЗ и чертежи
Владимир, здравствуйте! Прошу Вас прислать всю необходимую информацию на почту info@otlichnici.ru и написать что необходимо выполнить. Я посмотрю описание к заданиям и подскажу вам по стоимости и срокам выполнения.